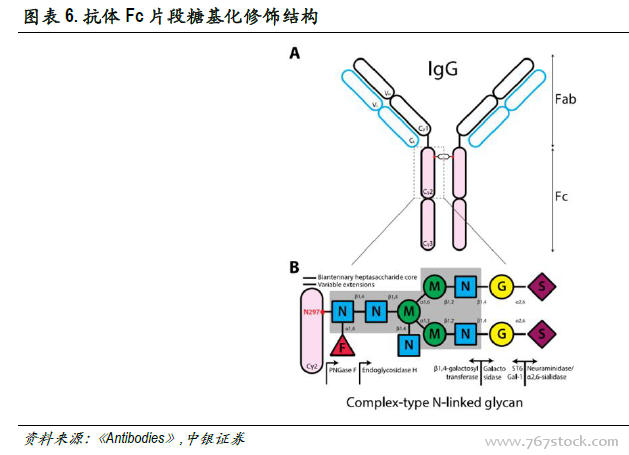
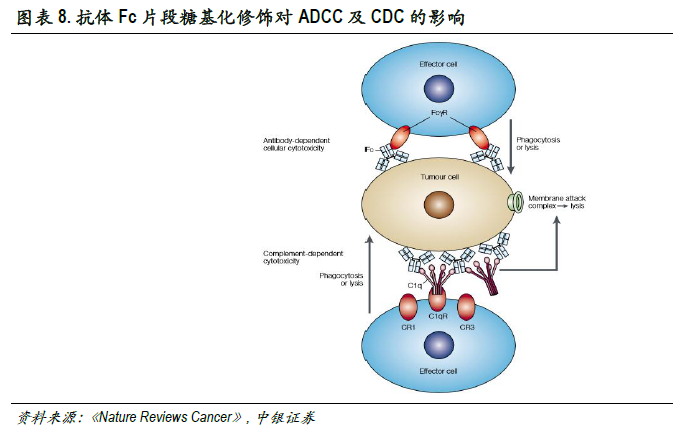
单抗Fc片段糖基化修饰显著强化单抗药物细胞毒作用。Fc片段通过活性区域与受体相结合发挥效应子功能。人类具有多种效应子配体(如FcyRs、C1q补体等),IgG的N-糖基化位于Fc片段的CH2区的共有序列(Asn297-X-Ser/Thr,X可以是除脯氨酸的任意氨基酸残基),通过酰胺键与抗体共价结合。Fc糖基化糖分子具有复杂的双天线型核心结构,该结构由甘露糖(Man)和N-乙酰葡糖胺(GlcNAc)两种戊糖分子组成,不同糖型除核心结构外还含有不同数目的糖分子,如岩藻糖(Fuc)、甘露糖、N-乙酰葡糖胺、半乳糖(Gal)、二等分N-乙酰葡糖胺和唾液酸(Sia)。
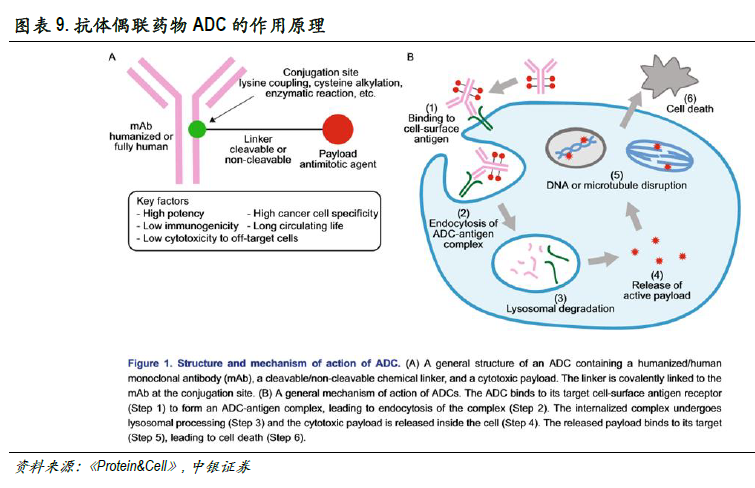
抗体偶联药物(ADC)可降低化药毒性,但制备技术仍是需要攻克的难点。抗体偶联药物(ADC),是一种将化学类药物通过连接物(linker)与抗体偶联形成的药物,进而降低化疗中常用药物非特异性的全身毒性。抗体偶联药物经过血液运输到达并识别癌细胞的表面抗原,其抗体部分与抗原结合后被内吞进入癌细胞内部并进一步在溶酶体中被剪切,释放有杀伤作用的化合物类药物(作用于DNA或细胞微管蛋白)。内吞化学类药物的细胞死亡裂解后,毒素分子会释放至附近的其他肿瘤细胞进一步发挥杀伤作用。
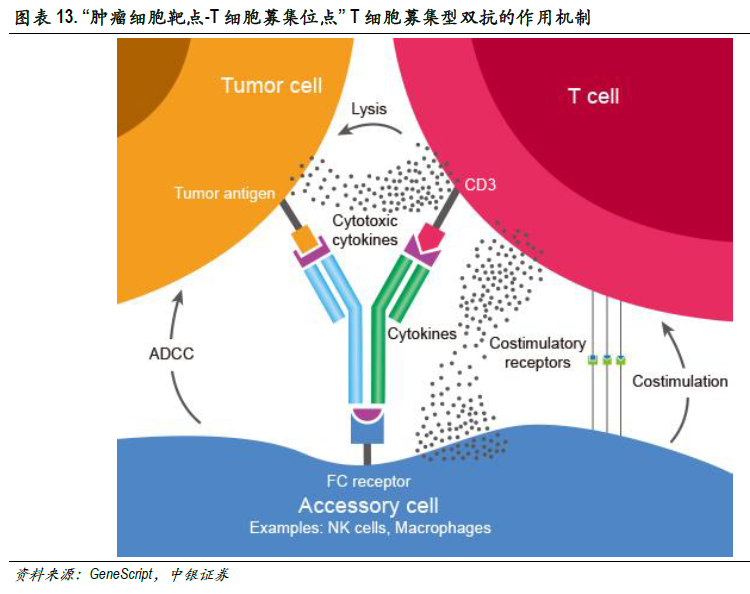
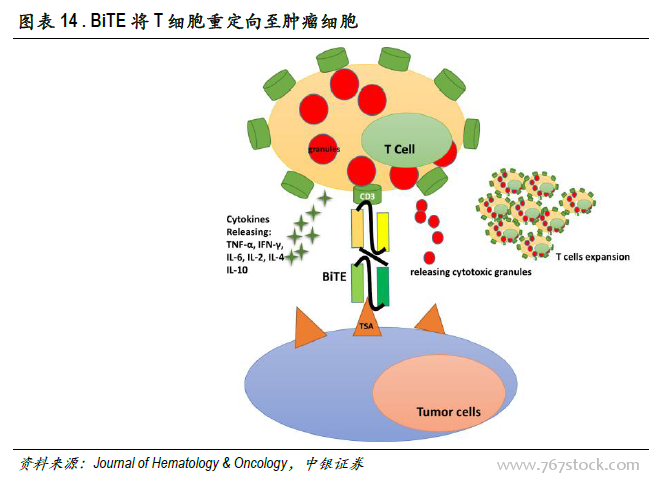
双特异性抗体具有“1+1>2”的肿瘤治疗效果。从靶点来源角度,双特异性抗体可以分为两种,即T细胞募集型和肿瘤双靶点结合型。肿瘤双靶点结合型可同时结合肿瘤细胞的两个靶点(如VEGF-PDGF、VEGF-Ang2),单克隆抗体通常只靶向一个抗原或一个表位,而某些疾病的发生常常与多条信号通路相关,导致疾病的复发,双抗可以抑制2条信号通路减少产生耐药的可能性。T细胞募集型双抗靶向肿瘤细胞靶点和T细胞募集位点,占双抗的大部分,T细胞募集位点一般靶向CD3(T细胞)、CD16靶点(NK细胞),可将T细胞重定向到肿瘤细胞,避免肿瘤细胞的免疫逃逸。
PD-(L)1单抗避免癌细胞的免疫逃逸,开启免疫治疗时代。由PD-1及其配体PD-L1、PD-L2组成的通路在维持外周免疫耐受中起着关键作用,而肿瘤也利用该途径从T细胞介导的特异性免疫中逃逸。T细胞处于激活状态时会进行代谢重编程,有氧糖酵解成为主导的代谢过程;谷氨酰胺的摄取和分解代谢也会增加,这些都是效应T细胞的适应性和记忆T细胞发育所需要的。肿瘤细胞通过PD-1抑制氧耗量,并削弱了活化T细胞参与糖酵解和分解谷氨酰胺的能力。当T细胞受到PD-1配体结合的刺激后,细胞内开始聚集公认的T细胞免疫抑制剂——大量的多不饱和脂肪酸。通过限制T细胞的正常代谢, T细胞的分化模式改变,导致效应T细胞(TEFF)和记忆T细胞(TM)的分化减弱、调节性T淋巴细胞(Treg)和耗竭T细胞(TEX)的分化增强。PD-L1作为癌细胞上的抑制受体,能将抗凋亡信号传递给癌细胞,癌细胞开始进行高度糖酵解,PI3K-Akt-Mtor通路活化水平升高,最终导致癌细胞的存活改善。
【免费下载】http://tinyurl.com/ydbqwzep
【备用下载】
 单克隆抗体行业深度报告-六大靶点看生物创新药.pdf
(8.15 MB, 需要: 5 个论坛币)
单克隆抗体行业深度报告-六大靶点看生物创新药.pdf
(8.15 MB, 需要: 5 个论坛币)




 雷达卡
雷达卡





 京公网安备 11010802022788号
京公网安备 11010802022788号







