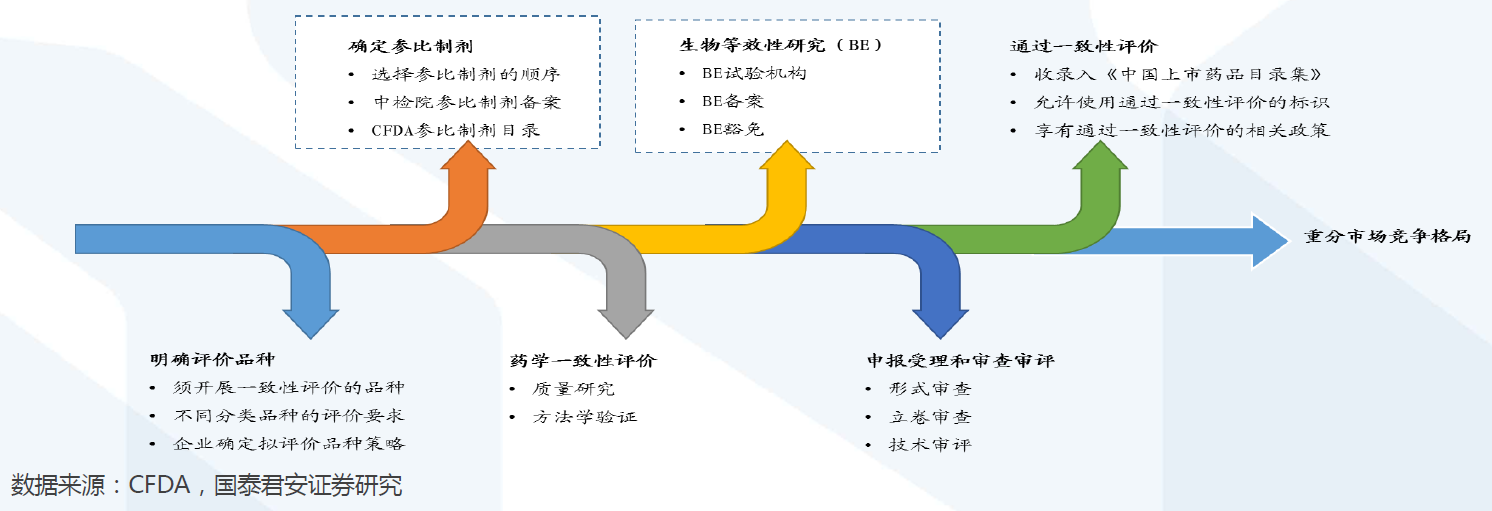
评价流程:确定参比制剂与开展BE试验是两大关键。开展仿制药质量和疗效一致性评价工作,要求已经批准上市的仿制药品, 在质量和疗效上与原研药品能够一致,临床上与原研药品可以相互替代。
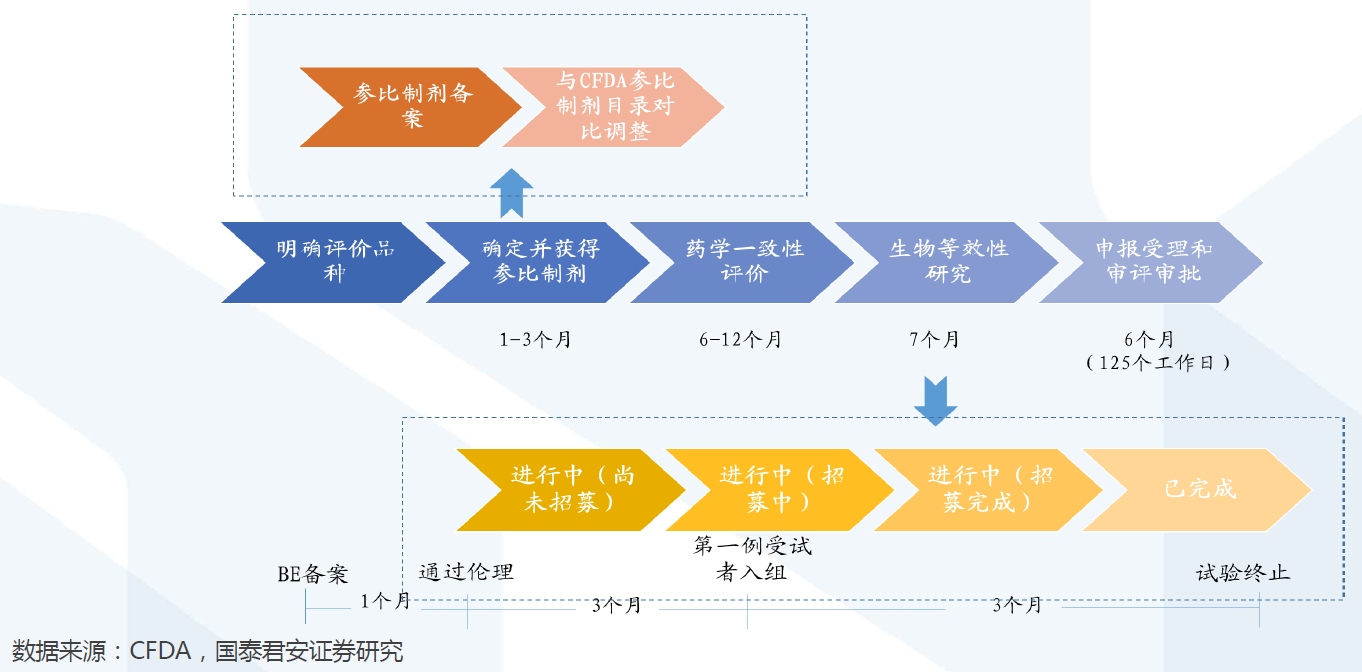
评价时间: 单个品种通过一致性评价周期约为20-28个月。单个品种通过一致性评价的周期约为20-28个月,其中:①确定并获得参比制剂需1-3个月;②开展药学一致性评价需6-12个月;③开展BE试验需7 月左右(从BE备案至试验终止);④申报受理和审评审批需6个月左右。

【免费下载】http://tinyurl.com/y7jnj3eu
【备用下载】
 医药行业专题报告-仿制药一致性评价展望.pdf
(7.67 MB, 需要: 5 个论坛币)
医药行业专题报告-仿制药一致性评价展望.pdf
(7.67 MB, 需要: 5 个论坛币)




 雷达卡
雷达卡





 京公网安备 11010802022788号
京公网安备 11010802022788号







